仭尋媶奣梫
1. 僸僩攟梴嵶朎傪梡偄偨僎僲儉埨掕惈堐帩婡峔偺夝愅
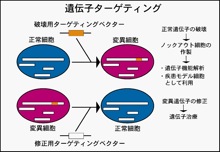
2. 幘姵儌僨儖僸僩堚揱巕僲僢僋傾僂僩嵶朎偺嶌惢偲夝愅
3. 曻幩慄傗峈偑傫嵻偵傛傞僎僲儉DNA懝彎偲偦偺廋暅婡峔偺夝愅
4. 崅岠棪僸僩堚揱巕僞乕僎僥傿儞僌媄弍偺奐敪
丂僎僲儉DNA偼丄揹棧曻幩慄傗妶惈巁慺丄庬乆偺峈偑傫嵻丄DNA暋惢僄儔乕側偳丄偝傑偞傑側撪揑丒奜揑梫場偵傛偭偰愨偊偢懝彎傪庴偗偰偄傑偡丅偙偆偟偨DNA偺彎偼堚揱巕敪尰傗堚揱忣曬偺堐帩丒揱払偵忈奞傪梌偊偰偟傑偄傑偡丅偙偺偨傔丄DNA偺彎傪恦懍偐偮惓妋偵廋暅偡傞偙偲偑嵶朎偺憹怋丒惗懚偵偲偭偰傕廳梫偱偡丅偦偺偨傔丄巹偨偪偺嵶朎偼丄僎僲儉DNA傪埨掕偵堐帩偡傞偨傔丄彎偺惗偠傞帪婜傗庬椶偵墳偠偨偝傑偞傑側DNA廋暅宱楬傪恑壔偝偣偰偒傑偟偨丅
丂偙傟傑偱偺尋媶偐傜丄DNA廋暅偵娭梌偡傞堚揱巕偑悢懡偔摨掕偝傟丄廋暅堚揱巕偺寚懝傗堎忢偑廳撃側堚揱昦傗偑傫偺尨場偲側偭偰偄傞偙偲傕傢偐偭偰偒傑偟偨丅偟偐偟側偑傜丄屄乆偺堚揱巕偺婡擻傗奺乆偺DNA廋暅宱楬偺徻嵶側暘巕婡峔偵偮偄偰偼埶慠偲偟偰懡偔偺撲偑巆偝傟偰偄傑偡丅
丂巹偨偪偺尋媶幒偱偼丄僸僩嵶朎偺僎僲儉DNA偑偳偺傛偆側巇慻傒偱埨掕偵堐帩偝傟偰偄傞偐傪柧傜偐偵偡傞偙偲傪堦偮偺栚昗偲偟偰丄堚揱妛揑丒嵶朎暘巕惗暔妛揑傾僾儘乕僠傪拞怱偵尋媶傪恑傔偰偄傑偡丅嬶懱揑偵偼丄巹偨偪偑嵟嬤撈帺偵奐敪偟偨僸僩堚揱巕僲僢僋傾僂僩僔僗僥儉傪棙梡偟偰丄DNA嵔愗抐廋暅偵娭傢傞僸僩堚揱巕傪僕乕儞僞乕僎僥傿儞僌朄偵傛偭偰攋夡偟丄摼傜傟偨僲僢僋傾僂僩曄堎嵶朎乮偙偺拞偵偼僸僩幘姵儌僨儖嵶朎傕娷傑傟偰偄傑偡乯偵偮偄偰徻嵶側昞尰宆夝愅傪峴偭偰偄傑偡丅偙偆偟偨尋媶偵傛偭偰丄屄乆偺廋暅堚揱巕偺嵶朎撪偱偺婡擻偺傒側傜偢廋暅堚揱巕娫偺堚揱妛揑側憡屳嶌梡傪柧傜偐偵偟偰偄偔偙偲偑偱偒傑偡丅
丂尰嵼偺曻幩慄椕朄傗壔妛椕朄偲偄偭偨偑傫帯椕偼丄抳柦揑側DNA懝彎傪恖堊揑偵桿敪偡傞偙偲偵傛偭偰偑傫嵶朎傪巰柵偝偣傞偙偲傪慱偄偲偟偰偄傑偡丅偟偐偟側偑傜丄偙偆偄偭偨帯椕朄偼懴惈摍偺栤戣偐傜廩暘側岠壥偑摼傜傟側偄堦曽丄惓忢側嵶朎傪傕彎偮偗偰偟傑偄傑偡丅巹偨偪偺尋媶偱摼傜傟偨僸僩嵶朎曄堎姅偼丄峈偑傫嵻側偳偺堛栻昳偺昡壙偵桳岠妶梡偡傞偙偲偑偱偒傑偡丅偮傑傝丄曻幩慄傗峈偑傫嵻偵傛偭偰惗偠偨DNA偺彎偵懳偟偰奺廋暅宱楬偑偳偺傛偆偵嫤挷偟偰廋暅傪峴偭偰偄傞偐傪柧傜偐偵偡傞偙偲偑偱偒傑偡丅偙偆偟偰DNA嵔愗抐廋暅婡峔偺慡懱憸傪懆偊傞偙偲偑偱偒傟偽丄傛傝岠壥揑偱暃嶌梡偺彫偝側偑傫帯椕朄傪奐敪偡傞偙偲偑壜擻偵側傞偱偟傚偆丅
丂巹偨偪偼丄DNA廋暅丒慻姺偊偺尋媶傪捠偠偰丄僕乕儞僞乕僎僥傿儞僌偺岠棪傪忋徃偝偣傞偨傔偺儊僇僯僘儉傕峫嶡偟偰偄傑偡丅憡摨慻姺偊偵傛傞僕乕儞僞乕僎僥傿儞僌傗旕憡摨慻姺偊偵傛傞儔儞僟儉僀儞僥僌儗乕僔儑儞偺儊僇僯僘儉傪夝柧偱偒傟偽丄擟堄偺僸僩嵶朎偵偍偄偰岠棪椙偔堚揱巕傪僲僢僋傾僂僩偡傞偙偲偑壜擻偵側傝傑偡丅傑偨丄埨慡側堚揱巕帯椕媄弍傊偺墳梡傕婜懸偱偒傑偡丅
仭2026擭搙偺庡側尋媶僾儘僕僃僋僩
1. 乽僎僲儉愗抐傪晄惓妋偵楢寢偡傞暋悢偺DNA廋暅婡峔偲偦偺惂屼偵娭偡傞曪妵揑棟夝偲墳梡乿丂暥壢徣壢尋旓 婎斦尋媶(A)
2. 乽TBA乿丂暥壢徣壢尋旓 挧愴揑朑夎尋媶乮枹掕乯
3. 乽僎僲儉埨掕惈堐帩偵偍偗傞儈僗儅僢僠廋暅偺婡擻夝柧偲偑傫帯椕傊偺墳梡乿丂崅徏媨斳娻尋媶彆惉婎嬥尋媶彆惉嬥
4. 乽儈僗儅僢僠廋暅偵傛傞慻姺偊惂屼偺儊僇僯僘儉偲墳梡乿丂忋尨婰擮惗柦壢妛嵿抍尋媶彆惉嬥



Go to Top.

